Sel volta komersial yang akan sobat Materi Kimia SMA
pelajari yaitu:
Sel Kering Baterai
Beberapa baterai yang sering sobat temui sehari-hari
diantaranya:
a)Baterai Seng-Karbon
Baterai jenis seng-karbon atau Leclanche adalah
baterai generasi pertama yang dikomersilkan, dipakai untuk lampu senter, jam
dinding, radio, dan alat-alat elektronik lainnya. Baterai ini terdiri atas seng
(anode) dan batang grafit (katode). Sebagai zat elektrolitnya adalah campuran
MnO2, NH4Cl, dan serbuk karbon yang dikemas dalam bentuk
pasta.
Reaksi redoks yang terjadi sangat rumit, tetapi secara
sederhana dapat ditulis dalam bentuk persamaan berikut.
Anode
|
:
|
Zn(s) → Zn2+(aq) + 2e–
|
Katode
|
:
|
2MnO2(s) + 2NH4+(aq) + 2e–
→ Mn2O3(s) + 2NH3(aq) + H2O(l)
|
Potensial sel yang dihasilkan adalah 1,5 V dan arus listrik
yang mengalir akan berkurang jika dipakai. Potensial sel juga akan berkurang
jika cuaca dingin.
b)Baterai Merkuri

Sel Volta yang lain adalah sel merkuri atau disebut juga
baterai kancing jenis Ruben-Mallory. Sel jenis ini banyak digunakan
untuk baterai arloji, kalkulator, dan komputer. Baterai merkuri ini telah
dilarang penggunaannya dan ditarik dari peredaran sebab bahaya yang
dikandungnya (logam berat merkuri).
Baterai kancing ini terdiri atas seng (anode) dan
merkuri(II) oksida (katode). Kedua elektrode tersebut berupa serbuk padat.
Ruang di antara kedua elektrode diisi dengan bahan penyerap yang mengandung
elektrolit kalium hidroksida (basa, alkalin). Reaksi redoks yang terjadi dalam
sel adalah sebagai berikut.
Anode
|
:
|
Zn(s) + 2OH–(aq) → ZnO(s) + H2O(l) + 2e–
|
Katode
|
:
|
HgO(s)+H2O(l)
+ 2e– → Hg(l) + 2OH–(aq)
|
Potensial sel yang dihasilkan adalah 1,35 V.
c)Baterai Litium
Sel kering tersebut (baterai seng-karbon dan baterai
merkuri) tidak benar-benar kering sebab elektrolit yang dipakai masih berupa
pasta. Sel kering yang benar-benar kering adalah sel jenis litium-iodin. Sel
litium-iodin adalah sel Volta dengan logam litium sebagai anode dan senyawa
kompleks I2 sebagai katode. Kedua elektrode ini dipisahkan oleh
lapisan tipis dari litium iodida. Reaksi redoks yang terjadi adalah sebagai
berikut.
Anode
|
:
|
2Li(s) →2Li+(aq) + 2e–
|
Katode
|
:
|
3I2(s) + 2e– → 2I3–(aq)
|
Potensial sel yang dihasilkan sebesar 3,6 V.
Baterai jenis litium berbeda dengan baterai seng-karbon dan
baterai merkuri sebab baterai ini dapat diisi ulang (rechargeable).
Baterai litium banyak dipakai untuk mobilephone (HP) dan mobil mainan.
d)Baterai Nikel-Kadmium
Selain baterai litium-iodin, baterai yang dapat diisi ulang
lainnya adalah baterai nikel-kadmium (nicad). Sel nicad adalah baterai untuk
penyimpan muatan. Sel nicad tergolong sel Volta yang terdiri atas kadmium
sebagai anode, nikel oksida sebagai katode, dengan elektrolit kalium
hidroksida. Baterai nicad banyak digunakan untuk baterai penerang isi ulang.
Reaksi sel selama pemakaian adalah sebagai berikut.
Anode
|
:
|
Cd(s) + 2OH–(aq) → Cd(OH)2(s)
+ 2e–
|
Katode
|
:
|
2NiO2H(s)+2H2O(l)+2e– → 2Ni(OH)2(s) + 2OH–(aq)
|
Sel Accumulator
Sel Volta komersial jenis lain yang dapat diisi ulang adalah
sel timbel atau dikenal dengan accumulator (accu), terdiri atas
timbel oksida sebagai katode dan logam timbel berbentuk bunga karang sebagai
anode. Kedua elektrode ini dicelupkan dalam larutan H2SO4
10%. Reaksi yang terjadi selama accu dipakai (discharged) adalah
sebagai berikut.
| Anode | : | Pb(s) + HSO4–(aq)
→ PbSO4(s) + H+(aq) + 2e– |
| Katode | : | PbO2(s) + 3H+(aq)
+ HSO4–(aq) + 2e– → PbSO4(s) + 2H2O(l) |
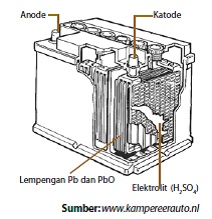
Potensial sel yang dihasilkan dari reaksi tersebut, yaitu
sekitar 2 V. Untuk memperoleh potensial sel sebesar 6 V, diperlukan tiga buah
sel yang disusun secara seri. Berapa jumlah sel yang harus disusun seri untuk menghasilkan
potensial sel 12 V?
Jika accu telah dipakai, accu dapat diisi
ulang menggunakan arus listrik searah. Selama proses isi ulang, reaksi dalam
sel merupakan kebalikan dari reaksi pemakaian. Reaksinya adalah sebagai
berikut:
2PbSO4(s)
+ 2H2O(l) → Pb(s) + PbO2(s) + 2H2SO4(aq)
Selama
proses isi ulang, sejumlah air dalam accu terurai menjadi H2 dan
O2, akibatnya accu kekurangan air. Oleh karena itu, accu yang
sering dipakai dan diisi ulang, cairan elektrolitnya harus diganti dengan yang baru.
Materi
Sel
Volta Komersial merupakan materi kimia kelas X terakhir
di Bab Reaksi Redoks. Jika sobat Materi Kimia SMA
akan mempelajari bab ini dari awal, silahkan menuju Pengertian Reaksi Redoks

